Исследование кинетики деградации антоцианов при портвейнизации в различных условиях
Study of the kinetics of anthocyanin degradation during aging of port wines under various conditions
Abstract: The port wine market is growing fastest within the fortified (liqueur) wine category, the production volume of which increased by 73.3% in Russia in January-June 2024, reaching 2.63 million liters. Red ports are the most popular, accounting for about half of the production volume. Anthocyanins, as the main pigments of red grape wines, undergo significant transformation at all stages of winemaking, including aging. The depth and intensity of such transformations play an important role in the formation of the color of the finished wine. The aim of this study was to investigate the degradation of anthocyanins during aging of ports under various conditions. During portization, the mass concentration of anthocyanins in the samples was determined using a Shimadzu UV-1800 spectrophotometer. As a result of four-factor analysis of variance, it was established that the greatest influence on the degradation of anthocyanins during port wine aging is exerted by the process temperature (the influence of the factor is 58.1%, p<0.01), the duration of port wine aging (the influence of the factor is 27.0%, p<0.01), the dosage of oak chips (the influence of the factor is 4.1%, p<0.01), the dosage of oxygen (the influence of the factor is 5.2%, p<0.01), as well as the combined influence of the factors “temperature × duration of port wine aging” (the influence of the factor is 2.4%, p<0.01). It was established that the degradation of anthocyanins corresponds to the kinetics of the first-order reaction, both in the experiment with and without microoxygenation. Based on the analysis of kinetic data, the activation energies of the anthocyanin degradation reaction were determined, as well as the pre-exponential factors of the Arrhenius equation depending on the aging mode of the ports.
Keywords: grapes, port wine, port wine aging, anthocyanins, degradation, kinetics, Arrhenius equations
Введение.
На сегодняшний день доля портвейнов в общем объеме производства крепленых вин составляет 35%. По данным Роскачества, выпуск портвейна удвоился в 2024 г. Рынок именно данного типа вина растет быстрее всего внутри категории крепленых (ликерных) вин, объем производства которой в январе-июне 2024 г вырос в России на 73,3 %, достигнув показателя 2,63 млн. литров. На первом месте по популярности – красные портвейны, на их долю приходится порядка половины от объема выпуска. Быстрый рост в категории демонстрируют и розовые портвейны, чья доля в объеме производства увеличилась по сравнению с прошлым полугодием на 10 %, до 13,4 % [1]. Эксперты Роскачества связывают рост производства портвейнов с возвращением интереса покупателей в целом к крепленым винам высокого качества, в том числе к выдержанным, марочным и коллекционным. Так же все большее значение для развития российского виноделия приобретают именно крепленые вина, особенности производства которых обуславливают лучшую стойкость готовых крепленых вин в процессе хранения и реализации.
Вышесказанное позволяет говорить о перспективах дальнейшего увеличения выпуска портвейнов в России, что делает крайне важным научное обоснование технологий портвейна из новых сортов винограда
В производстве портвейна традиционно выделяют несколько этапов, каждый из которых и их последовательность оказывают решающее влияние на стиль и качество конечного продукта. Эти этапы включают: выбор сорта винограда, сбор и дробление винограда, обработку (например, использование ферментов для интенсификации процессов сокоотдачи и осветления), спиртовое брожение, фортификацию этиловым спиртом различного происхождения и созревание (объединяет портвейнизацию и выдержку).
Одной из ключевых стадий производства портвейнов является тепловая обработка крепленых виноматериалов с целью ускорения их созревания, улучшения качества и придания типичных для портвейна органолептических свойств, а также выдержка в контакте с древесиной дуба течение от двух до 40 лет. Выдержка портвейна – сложный процесс, приводящий к снижению уровня многочисленных соединений, включая фруктовые этиловые эфиры в результате испарения и кислотно-катализируемых равновесных реакций. Наряду с последними активно протекают и обусловленные повышенной температурой окислительные процессы. Так, в результате исследований C.M. Oliveira и соавт. установлено, что антоцианы и флавоноиды катехинового типа являются соответствующими маркерами фенольного окисления в красных портвейнах. По мнению авторов, это истощение связано с преобразованием антоцианов в более стабильные цветные пигменты, что приводит к получению портвейнов с улучшенным цветом и меньшей терпкостью. Авторы также пришли к выводу, что температура, по-видимому, в большей степени влияет на кинетическую деградацию фенольных соединений, чем уровни кислорода, и предложили идентифицированные фенольные соединения использовать в качестве маркеров окисления. Таким образом, информация, полученная в ходе этих исследований, вполне может быть использована для оптимизации условий обработки вина и/или хранения [2].
На основании анализа доступных литературных данных, можно сделать вывод, что для формирования качества и характеристик портвейна во время портвейнизации важнейшими процессами, определяющими типичные цвет, аромат и вкусовой профиль, являются окислительные реакции (приводят к повышению уровня концентрации нескольких альдегидов и метилкетонов), а также другие механизмы, происходящие во время нагревания или хранения виноградного сока, – в частности, карамелизация и реакция Майяра [3], на интенсивность протекания которых влияет сочетание многочисленных факторов: продолжительность, pH, растворенный кислород, содержание SO2, но наибольшее влияние оказывает температура.
Антоцианы, как основные пигменты красных виноградных вин претерпевают значительную трансформацию на всех этапах виноделия, в том числе при выдержке. Глубина и интенсивность подобных превращений играет важную роль в формировании цвета готового вина. С химической точки зрения, наиболее важными реакциями антоцианов являются нековалентные взаимодействия (в основном, реакция копигментации), приводящие к стабилизации цвета, и также ковалентные взаимодействия, приводящие к образованию полимерных пигментов, отвечающих за большую часть цвета выдержанных вин [4].
Научное обоснование эмпирических знаний о возможностях использования нетрадиционных сортов винограда, вызревающих в условиях экстремального виноградарства и содействие микровиноделию портвейнов в условиях Алтайского края являются актуальными задачами, имеющими практическое значение как в рамках обеспечения продовольственной безопасности страны, так и для развития внутреннего туризма (в частности – энотуризма).
Целью настоящего исследования было исследование процесса деградации антоцианов при портвейнизации виноматериалов в различных условиях.
Объекты и методы исследования.
Виноград для исследований был выращен и собран в 2023 г. в Алтайском крае на опытном участке Бийского технологического института (филиала) ФГБОУ ВО «Алтайский государственный технический университет им. И.И. Ползунова» (с. Сростки Алтайского края, 52°25’00’’ с.ш.; 85°41’55’’ в.д., правый берег р. Катунь).
Образцы виноматериалов для исследований получали следующим образом. Виноград измельчали с использованием электрической дробилки-гребнеотделителя Rondinella (Италия, производительность 2000 кг/час). Для микробиологической стабилизации и предотвращения действия окислительных ферментов в мезгу вводили Kadifit (ERBSLÖH Geisenheim GmbH, Германия) из расчета содержания диоксида серы в мезге 100 мг/дм3. Сбраживание мезги при температуре 26-29 °С осуществляли дрожжами SafOeno™ VR 44 до содержания спирта в бродящей мезге не менее 6,0 %. Далее мезгу отделяли на корзиночном прессе, брожение останавливали добавлением спирта-ректификата до крепости не менее 18 % об. Спиртованные виноматериалы направляли на отдых для формирования дрожжевого осадка, который затем отделяли декантацией. Частично самоосветленные виноматериалы осветляли бентонитом, купажировали с сахарным сиропом до содержания сахаров 80 г/дм3 и направляли на портвейнизацию. Портвейнизацию осуществляли в контролируемых условиях: вариант 1 – без дозирования кислорода и без дозирования щепы дуба; вариант 2 – без дозирования кислорода, нос дозированием щепы дуба (2 г/дм3); вариант 3 – с дозированием кислорода (4 мг О2/дм3 в мес), но без дозирования щепы; вариант 4 – с дозированием кислорода и дубовой щепой.
Каждый вариант опыта (1-4) выдерживался в течение 10 недель при различных температурах хранения. Дозирование кислорода в образцы осуществляли при помощи микрооксигенатора (Enartis, Win-IQ, Италия) каждые 4 недели. Пробы анализировались еженедельно.
В ходе портвейнизации в образцах определяли массовую концентрацию антоцианов по методу В.Г. Гержиковой и использованием спектрофотометра Shimadzu UV-1800 [5].
Экспериментальные исследования проводили в пяти повторностях, результаты представляли как среднее значение ± стандартное отклонение. Статистическую обработку результатов исследований проводили с использованием пакета Statistica 10. Для оценки изменения содержания свободных антоцианов в образцах (В-1)–(В-4) использовали смешанную модель дисперсионного анализа, относя температуру портвейнизации, количество дубовой щепы и кислорода к фиксированным (контролируемым) факторам, а длительность портвейнизации к случайным факторам, т.к. невозможно с высокой точностью обеспечить выполнение исследования строго в одно и то же время каждые 168 часов (7 суток). Сравнение средних значений осуществляли с использованием теста Тьюки (p<0,05); сила влияния независимых переменных на изучаемый фактор оценивалась методом Снедекора (p<0,05).
Экспериментальная часть и обсуждение результатов.
Для получения портвейна виноград Зилга урожая 2023 г перерабатывали в соответствии с описанной схемой получения виноматериалов. Готовый крепленый виноматериал для портвейнизации имел активную кислотность 3,358±0,027 ед. рН, содержание сахаров составило 84,0±2,3 г/дм3, свободного диоксида серы – 20,6±1,9 мг/дм3, крепость виноматериала была 18,6±0,3 % об. Далее, виноматериал был разделен на 16 частей, помещен в герметичные сосуды, зашифрован и направлен на дальнейшие исследования соответствии с протоколом портвейнизации.
Результаты исследования динамики содержания антоцианов (в пересчете на мальвидин-3,5-дигликозид) при портвейнизации представлены на рисунке 1. Можно видеть, что портвейнизация при повышенной температуре способствует деградации антоцианов, которая, как отмечается в работе [6] может происходить по двум механизмам: 1) в результате гидролиза 3-гликозидной связи с образованием лабильного агликона и 2) в результате гидролитического раскрытия пириллиевого кольца с образованием замещенного халкона, который затем разрушается до коричневых нерастворимых фенольных соединений.
В результате четырех факторного дисперсионного анализа, установлено, что наибольшей силой влияния на деградацию антоцианов при портвейнизации оказывают температура процесса (сила влияния фактора – 58,1 %, p<0,01), длительность портвейнизации (сила влияния фактора – 27,0 %, p<0,01), дозировка дубовой щепы (сила влияния фактора – 4,1 %, p<0,01), дозировка кислорода (сила влияния фактора – 5,2 %, p<0,01), а также совместное влияние факторов «температура × длительность портвейнизации» (сила влияния фактора – 2,4 %, p<0,01). Иные возможные совместные взаимодействия изучаемых факторов в сумме имеют силу влияния не более 3,2 % (p<0,01). Отсутствие значимого совместного влияния всех четырех изучаемых факторов (сила влияния – 0,05 %, p<0,01) на процесс деградации антоцианов с методологической точки зрения может свидетельствовать о хорошей контролируемости эксперимента и возможности прогнозирования результатов.
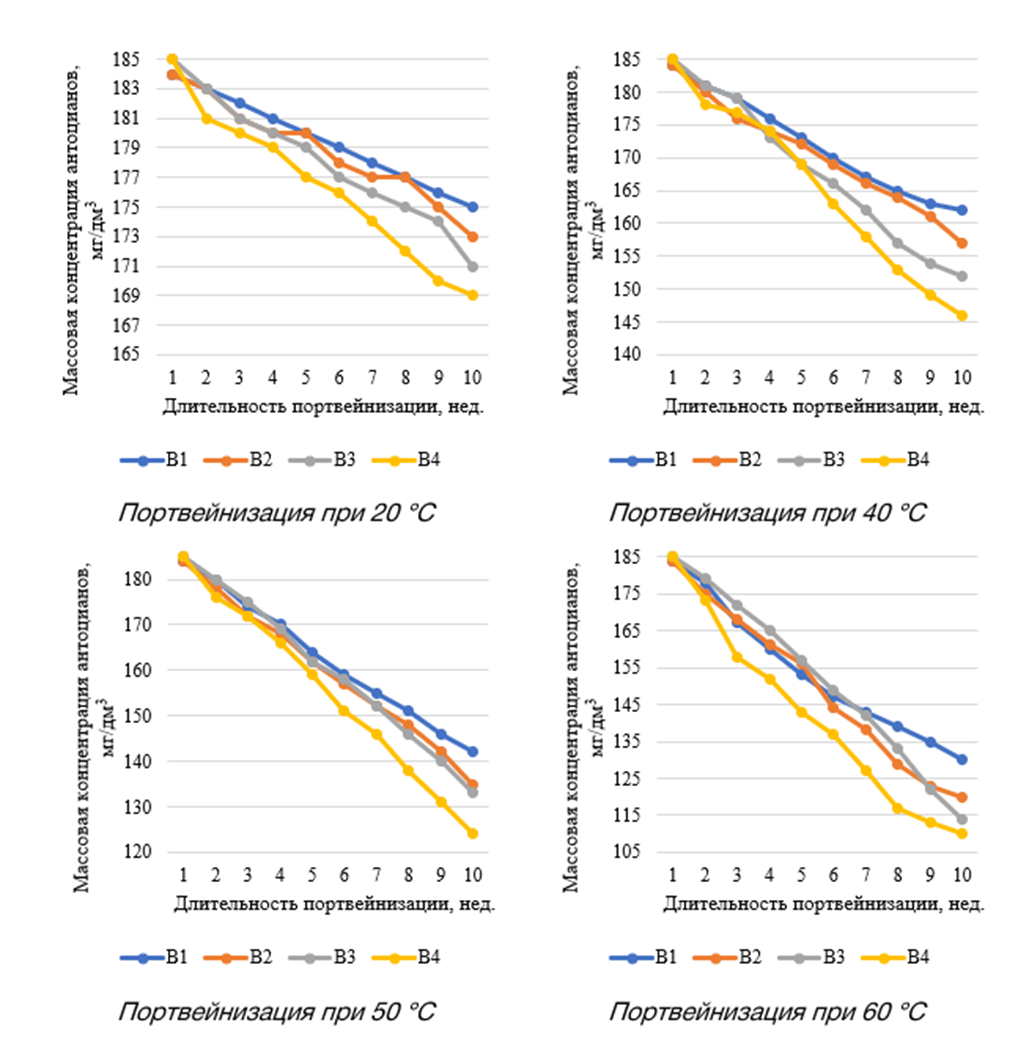
Рисунок 1 – Динамика содержания антоцианов при различных вариантах портвейнизации виноматериалов
В работах [7, 8] установлено, что потери свободных антоцианов при выдержке красных портвейнов подчиняются кинетике первого порядка. На основании экспериментальных данных было определен период полупревращения (t1/2) и рассчитаны индивидуальные скорости реакции разрушения антоцианов виноматериалов (k) в условиях опыта, используя соотношение: [9] (таблица 1).
Таблица 1
Константы скорости разрушения антоцианов и периоды полупревращений антоцианов
| Вариант опыта | k, ч-1 | t1/2, сут |
| В1-20 | 2,911×10-5 | 992 |
| В1-40 | 7,117×10-5 | 406 |
| В1-50 | 1,359×10-4 | 213 |
| В1-60 | 1,747×10-4 | 165 |
| В2-20 | 3,558×10-5 | 812 |
| В2-40 | 8,734×10-5 | 331 |
| В2-50 | 1,585×10-4 | 182 |
| В2-60 | 2,070×10-4 | 139 |
| В3-20 | 4,505×10-5 | 641 |
| В3-40 | 1,062×10-4 | 272 |
| В3-50 | 1,673×10-4 | 172 |
| В3-60 | 2,284×10-4 | 126 |
| В4-20 | 5,148×10-5 | 561 |
| В4-40 | 1,255×10-4 | 230 |
| В4-50 | 1,963×10-4 | 147 |
| В4-60 | 2,413×10-4 | 120 |
В предположении, что динамика разрушения антоцианов при портвейнизации подчиняется кинетическому уравнению первого порядка, концентрация антоцианов в процессе портвейнизайции может быть найдена из соотношения (1):
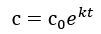
(1)
где с – концентрация антоцианов в момент времени t (ч), мг/дм3;
с0 – начальная концентрация антоцианов в виноматериале, мг/дм3;
k – константа скорости реакции, ч-1;
t – длительность портвейнизации, ч.
Зависимость константы скорости k от температуры T (К) выражается уравнением Аррениуса (2):
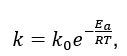
(2)
где k0 – предэкспоненциальный множитель, ч-1;
Еа – энергия активации, кДж/моль;
R – универсальная газовая постоянная (8,314 Дж/(моль×К)).
На основании обработки экспериментальных данных были построены диаграммы Аррениуса (рисунок 2) и определены энергии активации (Ea) и предэкспоненциальные коэффициенты (k0) для каждого варианта опыта (таблица 2).
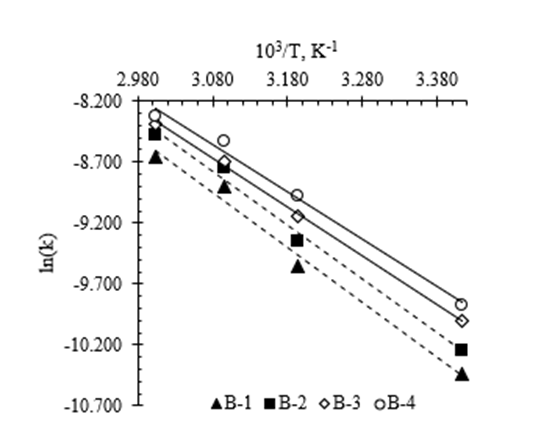
Рисунок 2 – Диаграммы Аррениуса для кинетики деградации антоцианов
Таблица 2
Коэффициенты уравнения Аррениуса
| Вариант опыта | Ea, кДж/моль | k0, ч-1 | R2 |
| В-1 | 36,336 | 102,89 | 0,9879 |
| В-2 | 35,712 | 95,14 | 0,9916 |
| В-3 | 32,927 | 35,57 | 0,9984 |
| В-4 | 31,330 | 23,02 | 0,9908 |
Фактически, температурная зависимость константы скорости реакции хорошо описывалась уравнением Аррениуса для всех вариантов портвейнизации. Максимальная деградация антоцианов отмечалась при более высоких температурах, и она соответствовала кинетике реакции первого порядка, как с добавлением кислорода, так и без него. Таким образом, зная кинетические параметры реакции термической деградации антоцианов и начальную концентрацию свободных антоцианов в портвейне можно предсказать состав антоцианов в вине в любой момент времени и при любой температуре используя уравнения 1 и 2 для каждого из режимов портвейнизации.
Полученные в эксперименте данные хорошо согласуются с результатами других исследователей. Так, в работе [10] рассмотрена кинетика деградации антоцианов при выдержке виноградных вин в бутылках в отсутствии кислорода. Авторы данного исследования пришли к выводу, что эволюция антоциановых пигментов при выдержке вина зависит не только от начальной концентрации антоцианов, но и от сортовых особенностей винограда (соотношения индивидуальных антоцианов).
В работе [6] авторами отмечалась сложность данных исследований из-за трудности учета всех факторов, участвующих в трансформации антоцианов портвейнов. Кинетический эксперимент, продолжавшийся в течение трех лет, показал, что три основные антоциана, содержавшиеся в опытных образцах были подвергнуты трансформации в значительном количестве, что коррелирует с полученными данными о периодах полупревращения антоцианов портвейна из винограда сорта Зилга при температуре 20 °С.
В работе [4] рассматривалась кинетика реакций пяти основных антоцианов виноградных вин в модельных растворах в диапазоне температур от 25 до 55 °С. В ходе исследования было доказано, что деградация антоцианов значительно увеличивается с повышением температуры, на основании чего были сделаны выводы о необходимости использования низких температур для стабилизации цвета при производстве и хранении виноградных вин.
Выводы.
На примере крепленого виноматериала из винограда сорта Зилга рассмотрены вопросы портвейнизации при различных условиях ведения процесса. Показано, что наибольшей силой влияния на деградацию антоцианов при портвейнизации оказывают температура процесса (сила влияния фактора – 58,1 %, p<0,01), длительность портвейнизации (сила влияния фактора – 27,0 %, p<0,01), дозировка дубовой щепы (сила влияния фактора – 4,1 %, p<0,01), дозировка кислорода (сила влияния фактора – 5,2 %, p<0,01), а также совместное влияние факторов «температура × длительность портвейнизации» (сила влияния фактора – 2,4 %, p<0,01). Установлено, что деградация антоцианов соответствует кинетике реакции первого порядка, как в опыте с микрооксигенацией, так и без нее. На основе анализа кинетических данных определены энергии активации реакции деградации антоцианов, а также предэкспоненциальные множители уравнения Аррениуса в зависимости от режима портвейнизации.
Библиографический список
1. Портвейн возвращается [Электронный ресурс] // Роскачество: портал для умного потребителя : [сайт]. 2024. URL.: https://rskrf.ru/news/portveyn-vozvrashchaetsya/ (дата обращения 12.12.2024).2. Oliveira, C. M. Influence of the temperature and oxygen exposure in red Port wine: A kinetic approach / C. M. Oliveira, A. S. Barros, A. C. S. Ferreira, A. M. Silva // Food Research International. – 2015. – Vol. 75. – P. 337-347. – DOI: 10.1016/j.foodres.2015.06.024.
3. Zhang, R. Evolution of nonenzymatic browning during the simulated Msalais‐production process in models of grape juice / R. L. Zhang, M. M. Zhang, Y. F. Pu, L. X. Zhu // Food Science & Nutrition. – 2022. – Vol. 10. – №. 7. – P. 2132-2140. – DOI: 10.1002/fsn3.2829.
4. Liu, Y. Reaction kinetics of the acetaldehyde-mediated condensation between (-)-epicatechin and anthocyanins and their effects on the color in model wine solutions / Y. Liu, X.-K. Zhang, Y. Shi, C.-Q. Duan, F. He // Food Chemistry. – 2019. – Vol. 283. – P. 315-323. – DOI: 10.1016/j.foodchem.2018.12.135.
5. Методы технохимического контроля в виноделии / под ред. В. Г. Гержиковой. – 2-е изд., перераб. и доп. – Симферополь : Таврида, 2009. – 304 с.
6. Silva Ferreira, A. C. 3-Hydroxy-4, 5-dimethyl-2 (5 H)-furanone: A key odorant of the typical aroma of oxidative aged port wine / A.C. Silva Ferreira, J. C. Barbe, A. Bertrand // Journal of Agricultural and Food Chemistry. – 2003. – Vol. 51. – №. 15. – P. 4356-4363. – DOI: 10.1021/jf0342932.
7. Bakker, J. The determination of anthocyanins in aging red wines: Comparison of HPLC and spectral methods /J. Bakker, N. W. Preston, C. F. Timberlake // American Journal of Enology and Viticulture. – 1986. – Vol. 37. P. 121–126. – DOI: 10.5344/ajev.1986.37.2.121.
8. Mateus, N. Evolution and stability of anthocyanin-derived pigments during Port wine aging / N. Mateus, V. De Freitas // Journal of Agricultural and Food Chemistry. – 2001. –Vol. 49. – P. 5217–5222. – DOI: 10.1021/jf0106547.
9. Harbourne, N. Determination of the degradation kinetics of anthocyanins in a model juice system using isothermal and non-isothermal methods / N. Harbourne, J. C. Jacquier, D. J. Morgan, J. G. Lyng // Food Chemistry. – 2008. – Vol. 111. – № 1. – P. 204–208. – DOI:10.1016/j.foodchem.2008.03.023.
10. Monagas, M. Evolution of polyphenols in red wines from Vitis vinifera L. during aging in the bottle: I. Anthocyanins and pyranoanthocyanins / M. Monagas, C. Gómez-Cordovés, B. Bartolomé // European Food Research and Technology. – 2005. – Vol. 220. – P. 607-614. – DOI: 10.1007/s00217-004-1108-x.
